Локальные спонсоры клинических исследований стали больше кодировать действующее вещество

По итогам прошлого года почти в каждом десятом локальном исследовании терапевтической эффективности и безопасности лекарственного препарата не указано действующее вещество, вместо этого в названии протокола фигурирует только его код. Среди тех, кто изучает биоэквивалентность, «маскировка» распространена еще больше: в 30% исследований. Об этом говорится в свежем выпуске Информационно-аналитического бюллетеня Ассоциации организаций по клиническим исследованиям (АОКИ), который имеется в распоряжении «ФВ».
Практика сокрытия действующего вещества с каждым годом набирает обороты, отмечают в АОКИ. Ассоциация обращала внимание на нее в своих отчетах с итогами 2023 и 2024 годов, однако с тех пор ситуация только усугубилась. Как ранее писал «ФВ», фармкомпании таким образом «маскируют» разрабатываемый препарат, чтобы не привлекать внимание потенциальных конкурентов к молекуле или терапевтической области и снизить риски судебных разбирательств с оригинатором.
«Мы считаем такую практику недобросовестной, а ее широкое распространение — маркером деградации отраслевых стандартов», — прокомментировала «ФВ» директор АОКИ Светлана Завидова.
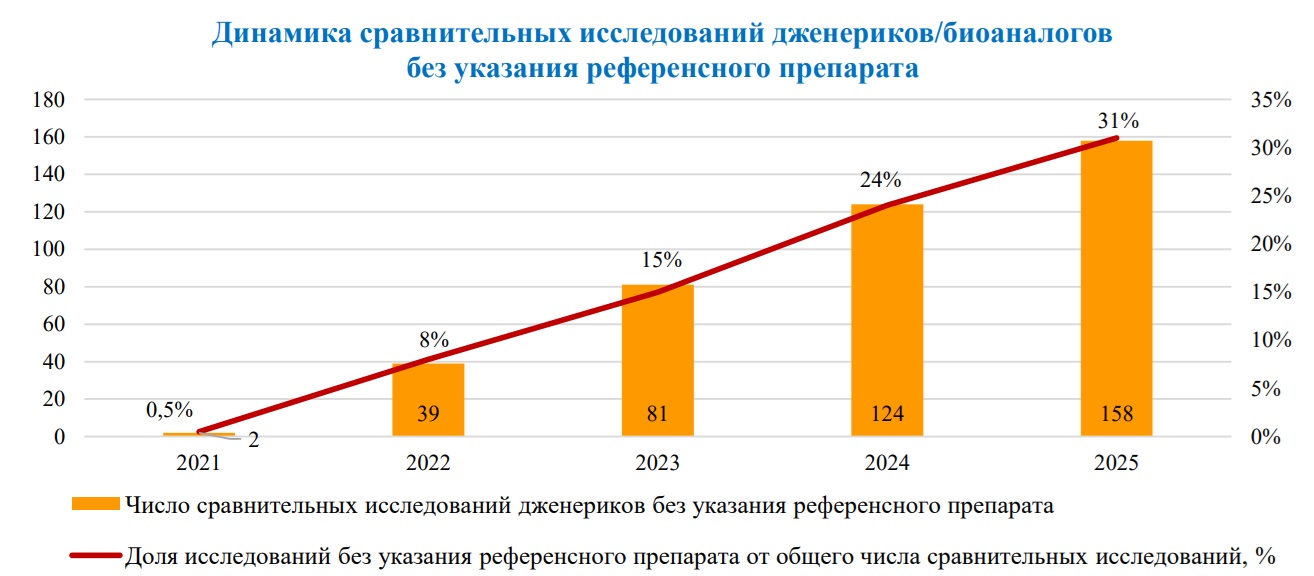
Данные: ГРЛС. Расчеты: АОКИ
В целом, по мнению эксперта, итоги 2025 года показывают, что российский рынок клинических исследований «обрел относительно устойчивую, но, возможно, не окончательную форму, главная характерная черта которой — аномально малая доля международных исследований».
Всего за 2025 год Минздрав России выдал 615 разрешений на запуск новых клинических исследований, на 2,2% меньше, чем в 2024 году (629 разрешений), следует из отчета. Наибольший вклад в снижение общего показателя внесло сокращение на 8,7% числа исследований биоэквивалентности, инициированных российскими спонсорами (313 против 343 годом ранее). Сгладить спад помог рост количества локальных исследований терапевтической эффективности и безопасности отечественных спонсоров (142 против 128, рост на 10,9%) и проектов иностранных компаний, преимущественно из Индии и Беларуси, по изучению биоэквивалентности (122 против 104, рост на 17,3%). При этом доля Индии уверенно увеличивается на протяжении последних пяти лет на фоне снижения доли европейских стран.
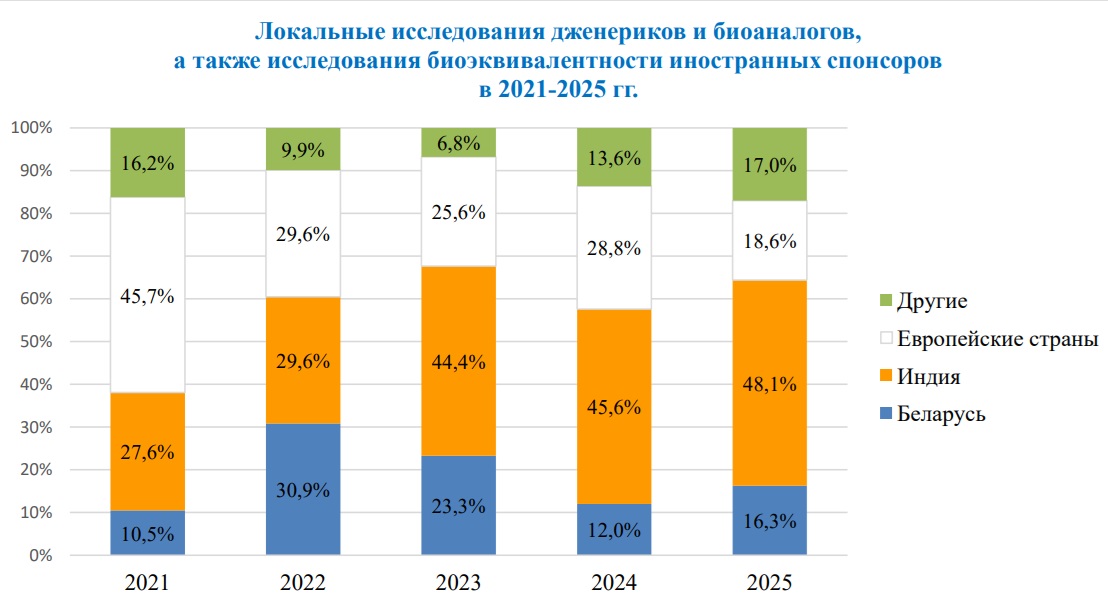
Данные: ГРЛС. Расчеты: АОКИ
Количество разрешений на международные мультицентровые клинические исследования (ММКИ) в 2025 году составило 22 против 18 годом ранее. Из них 11 инициировали российские разработчики с планами на открытие центров помимо России еще и в одной из стран-соседей, например, Беларуси или Казахстане, что отличает такие проекты по масштабу от глобальных международных протоколов, сказано в бюллетене.
| Почти половина всех ММКИ, разрешенных в 2025 году, относятся к онкогематологии и онкологии. |
Иностранные спонсоры получили 16 разрешений на локальные исследования. Преимущественно они разрабатывали дженериковые препараты и тестировали новые комбинации дженериков. 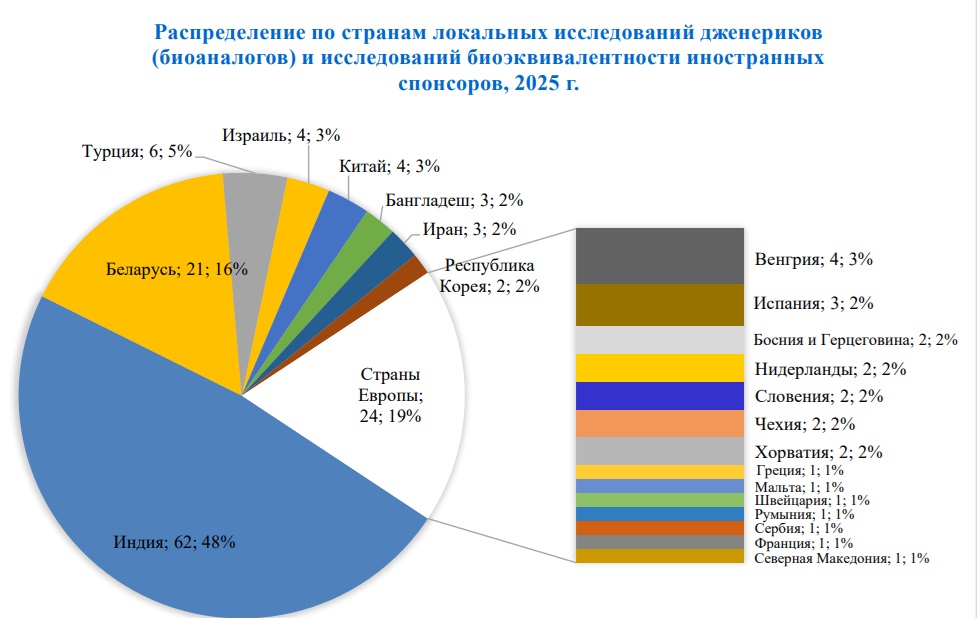
Данные: ГРЛС. Расчеты: АОКИ
На оригинальные биологические препараты пришлось только два разрешения иностранным спонсорам, столько же — на биоаналоги и на оригинальные малые молекулы.
Локальные спонсоры получили 142 разрешения на локальные исследования терапевтической эффективности и безопасности (без учета исследований биоэквивалентности). Наиболее крупная доля у биоаналогов — 31 протокол (21,8%). Эта категория впервые вырвалась вперед по итогам 2023 года и с тех пор не сдает позиции, оттеснив дженериковые препараты на второе место, говорится в отчете. Совокупная доля воспроизведенных биологических и небиологических лекарственных средств составила 44,4% всех локальных исследований отечественных спонсоров в 2025 году.
Оригинальные разработки представлены в 29 исследованиях (20,4%), из них 16 (11,3%) приходится на малые молекулы и 11 (7,7%) на биопрепараты. Еще по одному протоколу (0,7%) у комбинации оригинальной малой молекулы и дженериков, а также у комбинации оригинального биопрепарата с малой молекулой. Девять исследований (6,3%) пришлось на вакцины, по два (1,4%) на медицинские газы и на препараты крови, следует из бюллетеня.































Нет комментариев
Комментариев: