Минздрав резко сократил выдачу регистрационных удостоверений во время эпидемии
Выдача регистрационных удостоверений и внесение фармсубстанций в госреестр в мае значительно сократились относительно других месяцев и мая 2019 года (рис.). С момента объявления пандемии в марте и введения ограничений число регуляторных решений уменьшилось в 1,4 раза (табл.). Относительно мая прошлого года число новых препаратов сократилось в 2,4 раза.
Всего в мае Минздрав одобрил 26 лекарственных препаратов, в то время как год назад ведомство одобрило 61 препарат. В апреле и марте регистрационные удостоверения получили 44 лекарства.
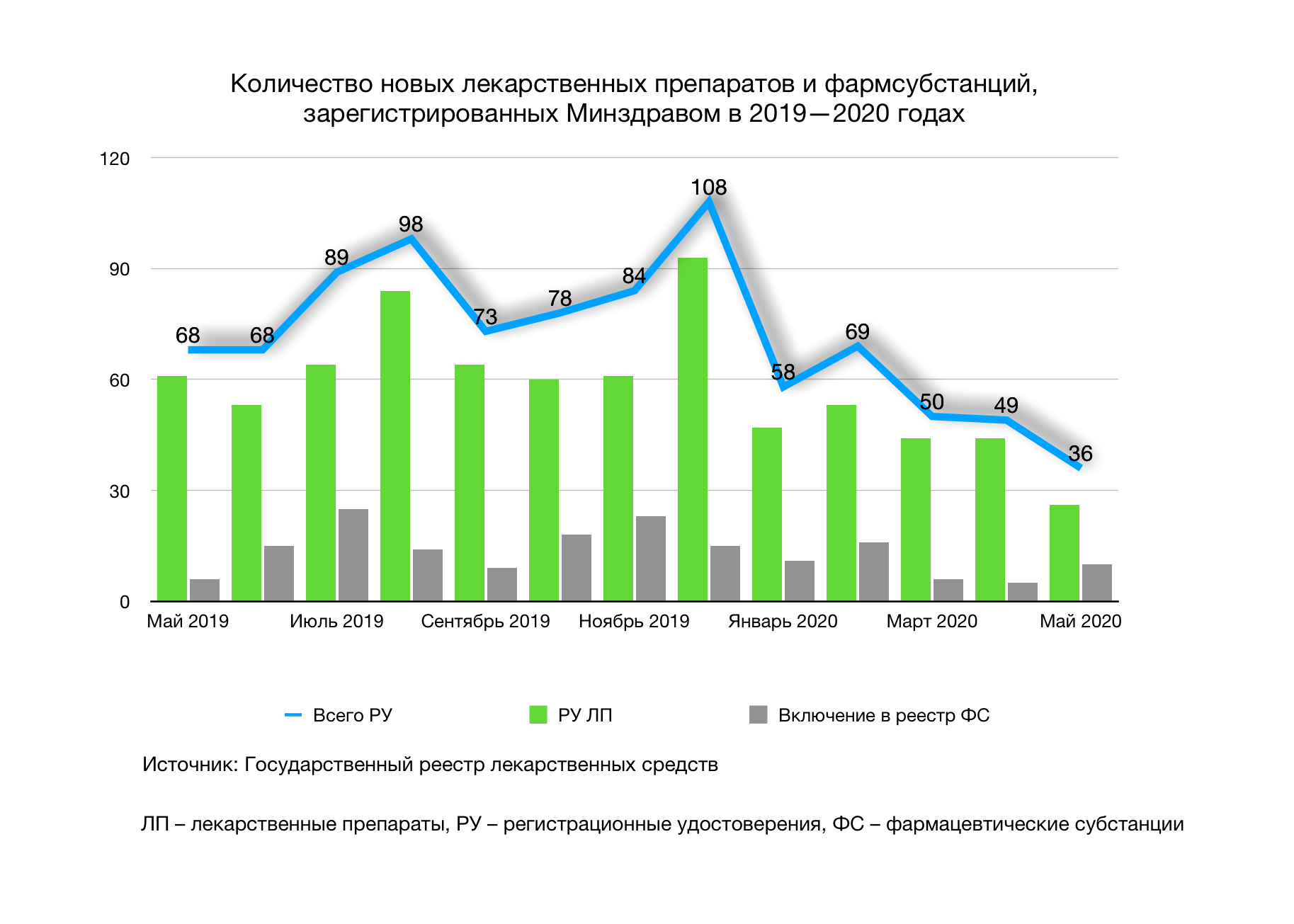
Таблица. Количество регуляторных решений Минздрава в 2019–2020 годах
|
|
Всего РУ |
РУ ЛП |
Включение в реестр ФС |
|
Май 2019 |
68 |
61 |
6 |
|
|
|
|
|
|
Январь 2020 |
58 |
47 |
11 |
|
Февраль 2020 |
69 |
53 |
16 |
|
Март 2020 |
50 |
44 |
6 |
|
Апрель 2020 |
49 |
44 |
5 |
|
Май 2020 |
36 |
26 |
10 |
Источник: Государственный реестр лекарственных средств
Сокращения: ЛП – лекарственный препарат, РУ – регистрационное удостоверение, ФС – фармацевтическая субстанция
Лончи препаратов в мае
На рынок РФ вышли три оригинальных препарата, два – компании «Р-фарм». «Дельтиба» (деламанид) разрешен для лечения туберкулеза с множественной лекарственной устойчивостью. Включен в список жизненно важных препаратов ВОЗ. Лекарство разработано компанией Otsuka Pharmaceutical Co. Права на производство и коммерциализацию на территории РФ и СНГ переданы в 2017 году компании «Р-фарм».
Олокизумаб «Артлегиа» одобрен для лечения ревматоидного артрита. В апреле начались клинические исследования олокизумаба при COVID-19. В июне препарат внесен во временные рекомендации Минздрава.
В мае регистрационное удостоверение получил этравирин «Интеленс» компании «Джонсон & Джонсон». Препарат разрешен для лечения ВИЧ-инфекции.
В мае экстренное одобрение получил фавипиравир компании «Кромис». Это первый препарат для лечения COVID-19 в России. Лекарство является аналогом оригинального фавипиравира японской компании Fujifilm.
Решение об одобрении «Авифавира» принято на основании постановления правительства об обращении препаратов в условиях чрезвычайной ситуации. Это указано в инструкции по медицинскому применению. Срок действия регистрационного удостоверения ограничен, истекает 1 января 2021 года. Применение фавипиравира возможно только в условиях стационара.






























Нет комментариев
Комментариев: 0