Парадокс лекарственной информации

Роза Ягудина, завкафедрой организации лекарственного обеспечения и фармакоэкономики Первого МГМУ им. И.М. Сеченова, проф., докт.фарм.наук
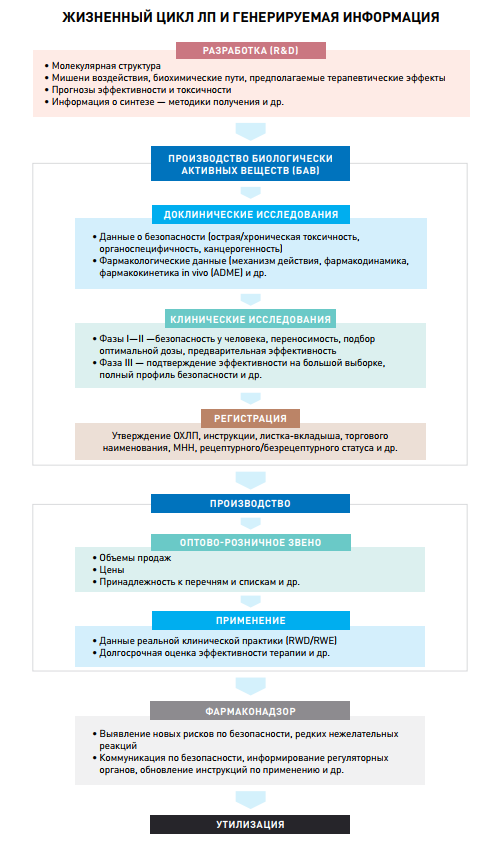
Что генерирует информацию
Основной пул лекарственной информации генерирует молекула-оригинатор. Именно она, проходя все этапы, собирает огромный массив данных, часть которого пойдет в регистрационное досье и будет представлена в регуляторно-экспертные органы.
Следующие за оригинатором воспроизведенные препараты (дженерики либо биоаналоги) также формируют некий пул синхронной с оригинатором информации, но с отдельными нюансами. Они зависят и от времени выхода на рынок препарата, и от актуальных требований регулятора на тот момент, и от планов компании-разработчика либо владельца регистрационного удостоверения.
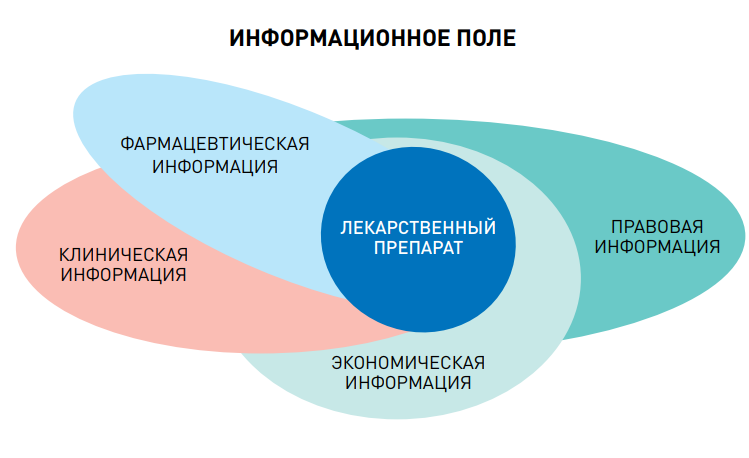
Оболочки информационного поля
Информационное поле лекарственного препарата включает несколько оболочек: клиническую (показания, противопоказания, побочные действия и др.), фармацевтическую (лекарственная форма, упаковка, условиях хранения и др.), экономическую, правовую. Выделить интеллектуальную собственность возможно, хотя в определенной степени ее можно отнести и к правовой составляющей.
Что должен знать потребитель
В информационном поле есть элементы, которые должны быть обязательно доведены до потребителей. Так, решением Совета Евразийской экономической комиссии № 881 утверждены требования к инструкции по медицинскому применению лекарственного препарата (листку-вкладышу) и общей характеристике, содержащей официальную информацию о препарате, предназначенную для медицинских работников в целях правильного назначения и контроля его применения.
Экономическая информация (цена лекарственного препарата) также должна быть доступна для населения. Зайдя в аптеку, мы можем ее увидеть на упаковке. Более того, в соответствии с действующими правилами надлежащей аптечной практики2 регламентировано, что покупателю должна быть предоставлена информация о наличии препарата с более низкой ценой (в рамках одного МНН).
|
5,6 млрд упаковок лекарственных препаратов ежегодно обращается на фармацевтическом рынке, по данным AlphaRM |
Следует отметить, что до недавнего времени была единая инструкция: и для населения, и для специалистов здравоохранения. Она находилась в каждой упаковке лекарственного препарата.
Значительная часть этого документа содержала термины и данные, которые были мало понятны человеку без специального образования. Сейчас в упаковках лекарственных препаратов вы уже найдете листок-вкладыш, который содержит понятную для населения информацию (в части упаковок ЛП содержится еще действовавший ранее формат, но к началу 2026 года все производители должны завершить переход на новые правила)3.
Есть даже специальные требования — как составлять эту информацию и как проверять, что население действительно правильно понимает, что написано в этой инструкции, так называемое пользовательское тестирование. И здесь на ум приходит фраза: «Все новое — хорошо забытое старое». Раньше в Советском Союзе в упаковки лекарственных препаратов были вложены как раз листки-вкладыши для населения.
Что должен знать специалист здравоохранения
Для специалистов здравоохранения теперь разрабатывается отдельная инструкция, или общая характеристика лекарственного препарата (ОХЛП), которая содержит гораздо больше информации, чем приведено в листке-вкладыше. Для отдельных препаратов ОХЛП может существенно превышать по объему листок- вкладыш.
Для сравнения возьмем листок-вкладыш (информация для пациента) и инструкцию ОХЛП (для специалиста здравоохранения) противоопухолевого препарата. Листок-вкладыш содержит чуть более 2,5 тыс. слов, инструкция ОХЛП — более 6,4 тыс. слов.
| В 90-е годы «личный формуляр» врача (ориентировочное количество лекарственных средств, которыми врач оперирует в своей профессиональной деятельности) насчитывал 60—80 МНН, сейчас он находится в интервале 150—300 МНН. |
С одной стороны, хорошо, что разделили объем и подачу лекарственной информации для населения и специалистов здравоохранения. Но, с другой стороны, врач не сможет теперь взять упаковку и посмотреть на листке-вкладыше данные, например, о фармакокинетике препарата. У него должен быть доступ к информационному ресурсу, в котором надо уверенно ориентироваться. Аптечному работнику немного проще — в аптеке практически всегда есть возможность заглянуть в информационную базу.
Про инструкции
Несмотря на то, что инструкция является неотъемлемой частью подаваемого на регистрацию досье на лекарственный препарат и проходит процедуру экспертизы, это не раз и навсегда застывший документ.
В нее периодически вносятся различные изменения (например, показания к применению, режим дозирования, взаимодействие, особенности применения отдельными группами пациентов и др.).
Особое внимание уделяется вопросам безопасности. Так, например, решением ЕЭК № 88 предписано регулярно пересматривать и обновлять раздел инструкции «Нежелательные реакции».
Но даже если компания это сделала, потребитель может не увидеть это в листке-вкладыше, так как этот бумажный вариант может быть уже устаревшим. Актуальная версия будет в электронном варианте. Но знает ли человек об этом?
Инструкции — это самый массовый источник информации о лекарственном средстве, вероятно, самый массовый источник печатной информации, которую читает население. Ежегодно на фармрынке обращается около 5,6 млрд упаковок лекарственных препаратов4. И в каждой упаковке должна быть инструкция.
Где найти официальную информацию о препарате
До последних лет был один официальный источник информации о лекарственных препаратах — Государственный реестр лекарственных средств. Сейчас добавился еще один — Единый реестр лекарственных средств Евразийского экономического союза.
Хотелось бы обратить внимание, что это официальные источники информации — именно они, а не всевозможные справочники.
Также следует иметь в виду, что ассортимент зарегистрированных препаратов постоянно расширяется, появляются новые данные по эффективности и безопасности, получаемые и после их регистрации.
Какая нужна информация
Специалистам здравоохранения важно получать актуальную информацию. Да, инструкцию на конкретный препарат они смогут найти. В конце концов можно предположить, что они смогут отследить последние изменения, заглядывая периодически в госреестр и реестр ЕАЭС. Но для лечения того или иного заболевания может применяться не один и не несколько, а десятки лекарственных препаратов.
Еще один нюанс. Зачастую есть несколько лекарственных средств (разные МНН), которые имеют схожий механизм действия. Для врача и провизора в такой ситуации важна сравнительная информация об этих препаратах. А еще и после регистрации лекарственного препарата продолжает накапливаться информация по различным аспектам его применения.
Недавно на одной из отраслевых аптечных конференций модератор дискуссии задал вопрос: как повысить активность первостольников в общении с посетителями аптеки при отпуске лекарств, как сделать, чтобы он активно разъяснял особенности применения лекарств и не боялся этого делать? Ответ: надо сформировать профессиональную уверенность аптечных работников. Это интересный в практическом плане профессиональный вопрос, требующий отдельного рассмотрения. Если же говорить о врачах, то и у них должна расти потребность в лекарственной информации.
Есть ряд публичных ресурсов, на которых размещена различная информация о лекарственных препаратах. Так, например, на сайте Росздравнадзора размещены данные о вводе лекарственных препаратов в гражданский оборот, контроле их качества и др.
Как информация доносится до врачей и фармспециалистов
На эту тему есть много исследований, в основном они посвящены предпочтениям врачей и аптечных работников по каналам получения информации: электронный, печатный и т.д. Но основные вопросы при этом, на мой взгляд: кто генерирует эту информацию, кто ее доводит и с какой целью?
Так получилось, что основным поставщиком информации о лекарственных препаратах сейчас являются по сути фармацевтические компании.
В начале 90-х годов перестала функционировать иерархически построенная система формирования и доведения информации о лекарственных препаратах до врачей и аптечных работников. Структурированная фармацевтическая информация доводилась от центрального уровня (ГАПУ республик) до аптечных управлений регионов, где были управления информации. Они, в свою очередь, доводили сведения до больниц и аптек. Были кабинеты фармацевтической информации в поликлиниках и даже должность — провизор-информатор. Эта система оказалась забытой и ненужной, а так как без информации работать невозможно, эту нишу заполнили фармкомпании.
Про доведение информации о лекарственных средствах до населения можно и не говорить. Есть только реклама. Понятного и объективного источника лекарственной информации для людей нет. Это предмет отдельного разговора, который с учетом доступности и качества информации в интернете явно недооценивается. Но такая ситуация не только в нашей стране.
В завершение приведу известное выражение: лекарственное средство — это есть лекарственное вещество плюс информация о нем.
В этом, пожалуй, и заключается парадокс: при стремительном развитии информационных технологий нужные сведения о лекарствах по-прежнему не всегда достигают тех, кому они действительно нужны.































Нет комментариев
Комментариев: 0